编者按:乳腺癌已成为我国女性发病率第一的癌种,其中HER2阳性乳腺癌约占1/4,曾一度以进展快、预后差著称。随着抗HER2诊疗策略的发展,多临床决策点、多靶向药物治疗模式将为HER2+患者争取最大化的治愈机会。《肿瘤瞭望》追寻HER2阳性乳腺癌全程管理策略,积极争取乳腺癌患者早期治愈,延长晚期生存。为汝,朝朝暮暮。
早期治愈:新辅助标准cT>1cm?
新辅助治疗的目的一方面是以手术为导向,另一方面是以敏感性信息判断为导向。早期乳腺癌新辅助治疗可以缩瘤降期,把不可手术的病人变成可手术,不可保乳的病人变成可保乳,不可保腋窝的病人变成可保腋窝,这是满足手术需求。另外新辅助治疗可以为基因检测留出时间,为更复杂的重建手术选择留出时间,其药敏信息可以提供调整辅助治疗方案的机会,早期治疗缓解使患者受到鼓舞,提高依从性。
随着国内外指南的更迭,新辅助治疗的适应人群在不断扩大。尤其是2021ASCO新辅助指南指出“T1a N0和T1b N0的HER2阳性乳腺癌患者不应常规接受新辅助化疗或抗HER2药物治疗”,言外之意即“T>1cm,N≥0,M0即可考虑新辅助治疗”,一石激起千层浪。纵观国内外指南,权衡患者治疗获益与伤害是新辅助治疗的核心精神之一,治疗不足和过量均不可取。临床中cN0的患者存在病理学阳性(cN0pN+)和病理学阴性(cN0pN-)两种可能,而在新辅助治疗前进行广泛的淋巴结活检是不合理的,因而在临床中无法准确的判断cN0患者真实的pN状态,所以为了防止对于cN0pN-过度治疗,根据cT判断患者是否接受新辅助治疗十分必要。
随着双靶时代的到来,临床专家普遍认可在新辅助治疗阶段,凡是符合单靶治疗的患者均可以考虑双靶治疗。目前,以PH双靶为基础的新辅助治疗方案可将tpCR稳定在60%以上,为患者带来明显获益。因此,国内外指南一直推荐HER2阳性乳腺其早期新辅助治疗优选双靶方案。

对于HER2阳性乳腺癌新辅助治疗后辅助治疗,若新辅助治疗阶段使用PH双靶,患者达到pCR,则继续使用PH双靶;若患者未达到pCR,则优选T-DM1,其次考虑继续使用PH双靶。2021年ESMO BC公布的BERENICE 5年最终分析,为HER2阳性乳腺癌从新辅助到辅助治疗全程PH双靶提供了一大力证。该研究显示,使用赫帕双靶为基础的新辅助方案联合剂量密集或蒽环类药物为基础的化疗,5年EFS率≥89.2%;4年IDFS率≥91.1%;5年OS率≥93.8%,心脏安全性良好,PH双靶全程应用为患者生存带来了极好的获益,实现治愈指日可待。

早期治愈:WSG-ADAPT研究带来豁免化疗的希望
双靶的兴起为豁免化疗提供了机遇,然而如何从HER2+的人群中筛选出此类人群至关重要。WSG-ADAPT HER2+/HR-研究对HER2阳性乳腺癌患者分别予以PH双靶(A组)和PH双靶联合12周紫杉醇(B组)。结果显示,包括原位癌在内,A组 vs B组 pCR率为90.5% vs 34.4%,同时A组取得pCR人群与B组pCR人群5年iDFS率均为98%,意味着该34.4%的患者豁免化疗可以取得良好结果。通过基因分析发现,HER2 3+、非基底样、早期缓解者、以及免疫信号相关预测性RNA信号表现患者可以从PH双靶治疗获益,似乎预示着此类人群可以豁免化疗。未来需要进一步更大规模的研究予以证实,期待能有明确的生物标志物得到确证,以帮助临床中豁免化疗的决策实施。

国内外指南一致强调,延长患者生存是晚期乳腺治疗的主要目标,需根据临床决策点制定晚期诊疗策略。

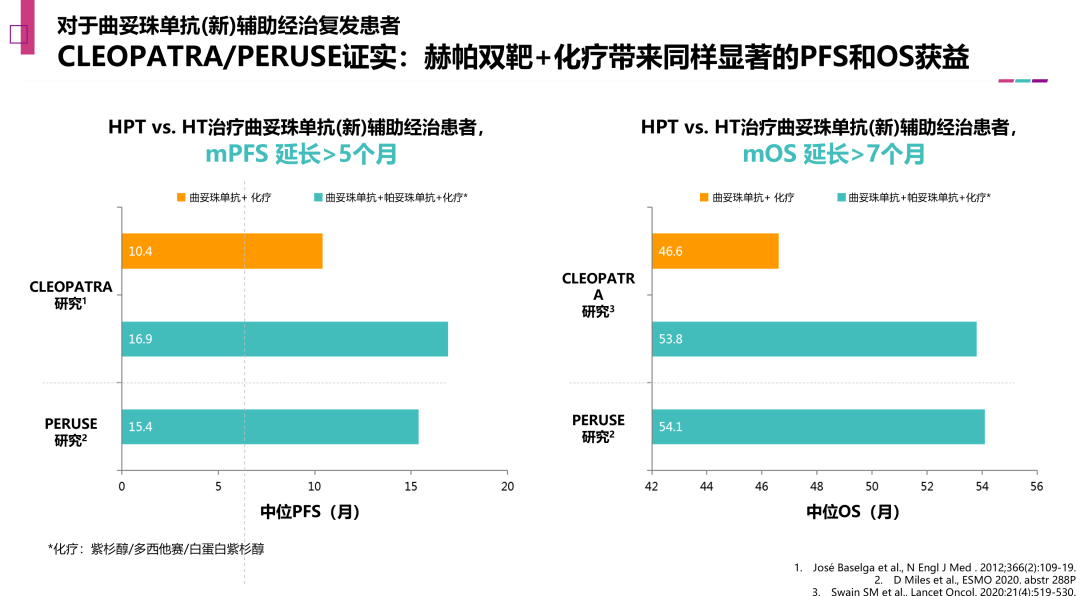
21世纪初,H0648g、M77001、HERNATA等研究奠定了曲妥珠单抗±化疗一线治疗HER2阳性晚期乳腺癌的标准地位。帕妥珠单抗问世后,CLEOPATRA研究以惊艳的57.1个月的OS将PH双靶送上指南一线治疗金标准。因此,对于未经曲妥珠单抗治疗的患者,应优选PH+化疗的一线方案。

对于接受过曲妥珠单抗(新)辅助治疗的患者,若治疗后>12个月复发,CLEOPATRA/PERUSE对经治患者的数据分析证实PH双靶较单靶可延长患者mPFS 5个月以上,延长mOS 7个月以上。此外,COMACHI研究、RePer研究等均对此进行了进一步证实。所以,此类患者一线也应优选PH双靶方案。
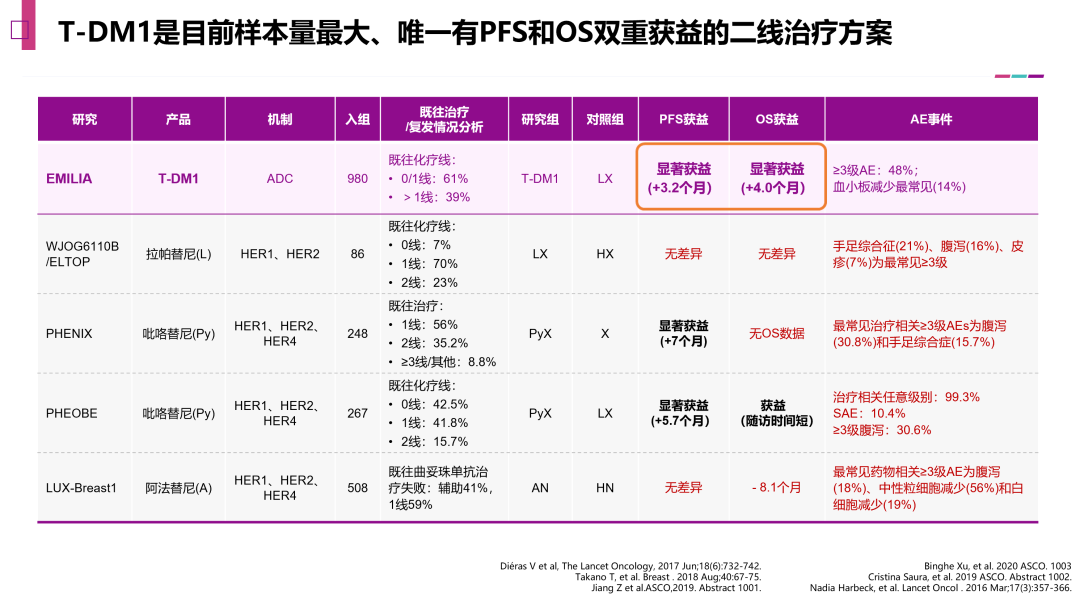
若患者在接受曲妥珠单抗(新)辅助治疗后12个月内复发,则需要考虑二线抗HER2治疗,在TKI、ADC等多种药物选择中,T-DM1是目前样本量最大,唯一有PFS和OS双重获益的二线治疗方案,成为指南推荐的二线标准选择。
晚期生存:HER2阳性晚期脑转移乳腺癌系统治疗策略
在 HER2阳性晚期乳腺癌患者中,颅脑是最常见的转移部位之一,脑转移的发病率约为 30%-55%,严重影响患者生存,各大指南往往以手术或放疗等局部治疗作为主要推荐手段。曾有Ⅱ期临床研究显示拉帕替尼联合卡培他滨针对脑转移患者mOS为17个月;HER2CLIMB研究则显示图卡替尼联合曲妥珠单抗和卡培他滨对脑转移患者mOS达到21.9个月;在EMILIA研究的探索性分析中,对于脑转移患者,T-DM1组较拉帕替尼联合卡培他滨组OS延长近1倍,mOS 26.8个月 vs 12.9个月(HR=0.382,95%CI 0.184-0.795,P=0.0081),是目前在脑转移患者中取得最长OS的临床研究。KAMILLA研究则进一步证实了T-DM1治疗HER2阳性脑转移乳腺癌疗效,43%的患者脑靶病变减少≥30%。因此,若HER2+脑转移晚期乳腺癌患者有系统治疗机会,T-DM1仍是有效的治疗选择。

晚期生存:PI3K-AKT通路组成性活化突变的应对
PIK3CA突变导致PI3K激酶组成性活化,在患者固有耐药和获得性耐药中可能均有作用,在HER2过表达乳腺癌中的发生率约为25%;同时PTEN功能缺失会通过PI3K-AKT生存通路导致持续信号传导活动,致使肿瘤耐药,在HER2过表达乳腺癌的发生率约为35%。对于此类耐药患者,ADC药物给了很好的解决思路,以T-DM1为例,其保留曲妥珠单抗特异作用机制,通过胞吞靶向药向细胞内传递,释放化疗药物DM1发挥杀灭肿瘤的作用,从而克服了该耐药机制。对此,EMILIA研究亚组分析证实,对于PIK3CA突变和野生型,T-DM1治疗后mPFS分别为10.9个月vs 9.8个月;对于PTEN蛋白缺失型和正常型,T-DM1治疗后mPFS费被为8.4个月 vs 9.9个月,且均优于对照组拉帕替尼联合卡培他滨的表现,为临床提供了诊疗思路。







 京公网安备 11010502033352号
京公网安备 11010502033352号